氟化修饰D-肽放射性药物联合免疫检查点阻断疗法的协同抗肿瘤效应研究
2026-04-07

研究背景
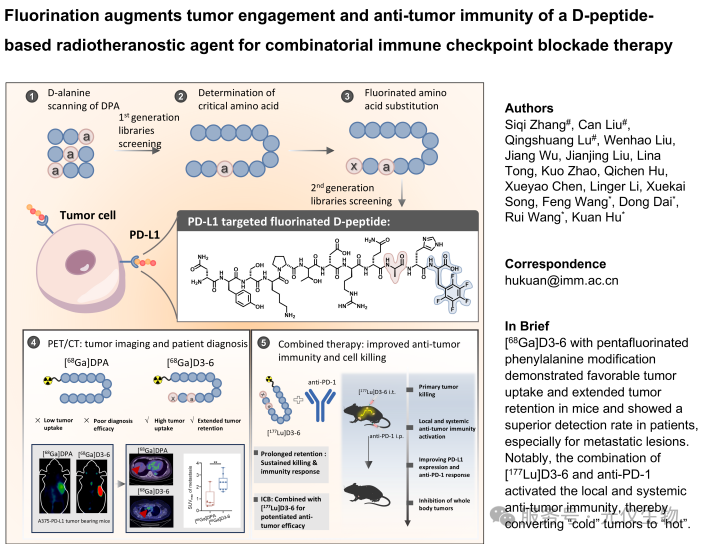
研究策略与分子优化
临床前及临床评价
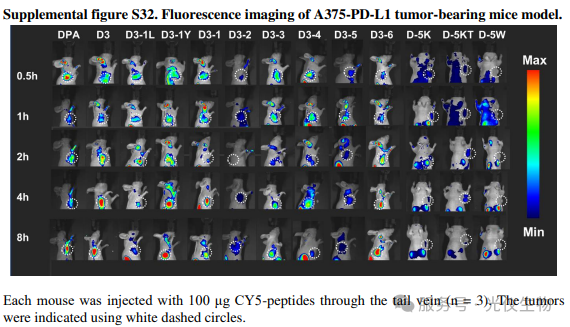
图为光仪小动物活体荧光成像系统拍摄的A375-PD-L1荷瘤小鼠模型荧光成像图(补充图S32)
协同治疗与免疫机制
研究结论与意义
文章信息

研究背景

研究策略与分子优化
临床前及临床评价

图为光仪小动物活体荧光成像系统拍摄的A375-PD-L1荷瘤小鼠模型荧光成像图(补充图S32)
协同治疗与免疫机制
研究结论与意义
文章信息
Copyright @ 2026 广州光仪生物科技有限公司 版权所有 ICP备案编号:粤ICP备17113150号