肺血管内皮EVs如何抑制Treg?研究揭示Med1-IL21信号轴关键作用
2026-03-19
急性呼吸窘迫综合征(ARDS)是重症监护室中常见的危重疾病,死亡率高达40%。调节性T细胞(Tregs)在肺部的减少导致炎症失控和恢复延迟,但背后的机制尚不明确。

研究背景
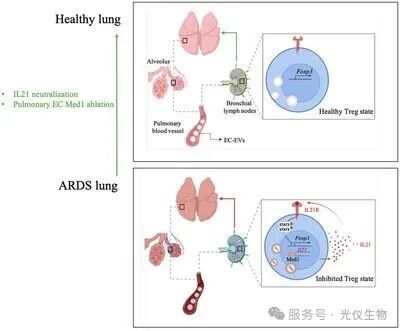
研究内容与发现
研究意义
文章信息
发表期刊:Journal of Extracellular Vesicles
影响因子:14.5(Journal of Extracellular Vesicles期刊网站官方数据,截止至2026年3月)
第一作者:刘旭、黄蔚、张曦文
通讯作者:谢剑锋、郑明珠、巢杰、邱海波
DOI:10.1002/jev2.70235
本文由光仪生物解读,我们很荣幸能为该项研究提供凝胶成像系统,助力科学发现。